Tabel Unsur Periodik Kimia - Dalam kehidupan sehari-hari, kita tidak lepas dari berbagai macam bahan kimia. Setiap jenis zat kimia tersebut memiliki sifat yang berbeda berdasarkan sifat periodiknya.
Bersumber dari Modul Kimia Kelas X MIPA Kemendikbud Ristek, sifat periodik untusr adalah sifat-sifat yang mempunyai kecenderungan untuk berubah secara teratur sesuai dengan kenaikan nomor atom, dalam periode periode yang sama dan dalam golongan yang sama.
Sifat-sifat peridoik unsur diantaranya adalah:
- Jari-jari atom yaitu jarak dari inti atom hingga kulit terluar elektron
- Energi ionisasi yaitu minimal energi yang diperlukan untuk melepaskan satu elektron dari suatu atom netral/ion dalam wujud gas
- Afinitas elektron yaitu besarnya energi yang diperlukan ketika mengikat satu elektron dari bentuk atom netral dalam wujud gas sehingga terbentuk ion dengan muatan -1.
- Elektronegatiitas yakni kemampuan atom untuk menarik elektron ke dalam ikatannya ketika atom tersebut membentuk ikatan.
- Logam dan non-logam.
Baca Juga: Sejarah Singkat dan Tokoh yang Terlibat di Serangan Umum 1 Maret 1949
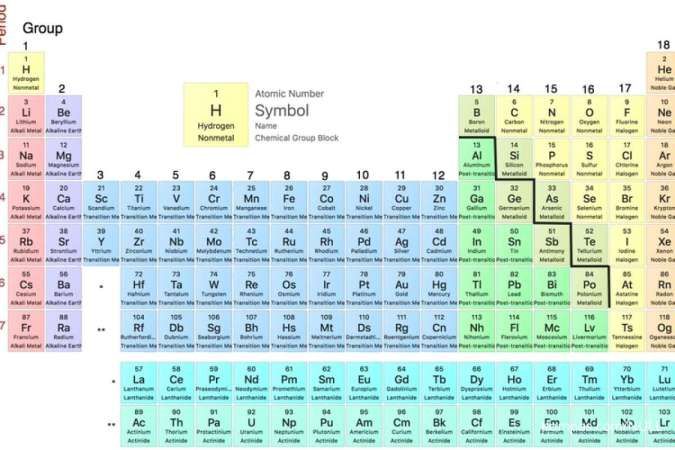
Tabel periodik unsur dan cara membacanya
Dalam tabel periodik unsur terdapat bagian-bagian yang perlu dipahami oleh siswa. Bagian-bagian dari tabel periodik unsur, mengutip Modul Kimia Paket C Kemendikbud Ristek yakni:
- Periode yang berada pada lajur horizontal sistem periodik unsur. Bagian ini disusun berdasarkan jumlah kulit yang dimiliki unsur
- Golongan yang beradi di lajur vertikal pada sistem periodik unsur. Bagian ini disusun berdasarkan jumlah elektron balensi unsur. Dalam satu golongan sifat unsur memiliki kemiripan.
Sistem periodik dan tabel periodik yang kita pakai saat ini adalah sistem periodik modern yang dicetuskan oleh Henry G. Moseley.
Pengelompokan unsur sistem periodik ini menyempurnakan hukum peridik sebelumnya yakni sistem periodik yang ditemukan oleh Dmitri Ivanovich Mendelev.
Sistem periodik modern memiliki 7 periode dan 8 golongan.
Kemudian masing-masing golongan dibagi lagi menjadi 8 golongan A yaitu IA-VIIIA yang disebut dengan golongan utama dan 8 golongan B yaitu IB-VIIIB yang disebut golongan transisi.
Melasir Modul Pembelajaran Kimia Madrasah Aliyah (MA) Kemenag, golongan A atau utama memiliki sebutannya masing-masing sesuai dengan nomor golongan, yaitu:
- Golongan IA = alkali elektron
- Golongan IIA = alkali tanah
- Golongan IIIA = aluminium
- Golongan IVA = karbon elektron valensi
- Golongan VA = nitrogen elektron valensi
- Golongan VIA = oksigen/kalkogen elektron valensi
- Golongan VIIA = halogen elektron valensi
- Golongan VIIIA = gas mulia elektron valensi
Sedangkan golongan B semuanya adalah transisi sehingga tidak memiliki penamaan khusus untuk masing-masing nomor golongan.
Untuk periode, berikut ini penjelasan masing-masing periode dalam tabel periodik unsur:
- Periode 1, terdiri dari 2 unsur
- Periode 2, terdiri dari 8 unsur
- Periode 3, terdiri dari 8 unsur
- Periode 4, terdiri dari 18 unsur
- Periode 5, terdiri dari 18 unsur
- Periode 6, terdiri dari 32 unsur (termasuk deret Lantanida)
- Periode 7, terdiri dari 32 unsur (termasuk deret Aktinida)
- Periode 6 deret Lantanida, terdiri dari 14 unsur dengan nomor atom 58-71
- Periode 7 deret Aktinida, terdiri dari 14 unsur nomor atom 89-103
Baca Juga: 5 Faktor yang Mendorong Perdagangan Internasional antar Negara
Deret Lantanida dan deret Aktinida, keduanya masuk dalam golongan IIIB. Lalu mengapa tabel periode Deret Lantanida dan deret Aktinida berada di tabel yang terpisah meskipun masuk pada golongan IIIB?
Penempatan unsur-unsur pada kedua golongan tersebut sebenarnya untuk alasan teknis sehingga daftar tidak terlalu panjang. Oleh sebab itu deret Lantanida dan Aktanida berada di bagian bawah tabel.
Cara membaca tabel periodik unsur sebenarnya cukup mudah mengingat unsur-unsur sudah berada di golongan/periode yang sama. Dalam satu kotak unsur terdapat keterangan berupa:
- Nomor atom dari 1-103
- Masa atom
- Simbol unsur
- Nama unsur
Selain itu unsur-unsur kimia dalam tabel periodik juga sudah tersusun berdasarkan nomor atom. Semakin ke bawah dan ke kanan, semakin besar nomor atom dan semakin berat massa atom suatu unsur.
Pada tabel periodik unsur terdapat juga keterangan warna. Masing-masing golongan memiliki warna yang sama yang menunjukkan sifat golongan unsur tersebut.
Kemudian unsur-unsur logam, non-logam , dan semi logam biasanya berada di golongan yang sama kecuali Hidrogen.
Unsur logam biasanya berada pada kiri tabel kecuali Hidrogen yang masuk dalam unsur non logam. Selanjutnya pada bagian kanan tabel pada umumnya adalah unsur non logam. Diantara unsur logam dan non logam terdapat unsur semi logam.
Cek Berita dan Artikel yang lain di Google News
/2024/03/01/92523295.jpg)









